Page 1 sur 1
Synthèse de la mauvéine
Publié : 22/05/2020, 15:07
par Polochon
Bonjour,
Est-ce que par hazard quelqu'un saurait quels sont les outils de laboratoires ou industriels pour la synthèse de la mauvéine, ou même la synthèse des colorants en général
Merci beaucoup

Re: Synthèse de la mauvéine
Publié : 23/05/2020, 14:48
par Maurice
Comme tu sembles vouloir te lancer dans une opération délicate, le plus simple pour toi me paraît d'aller sur Google, et de taper Mauvéine. Tu trouveras des quantités d'articles consacrés à ce sujet, dont le premier est bien entendu le résultat de la recherche sur Wikipedia. Vas-y voir ! C'est encore ce qu'il y a de plus simple et de plus efficace.
Re: Synthèse de la mauvéine
Publié : 25/05/2020, 11:51
par ecolami
Bonjour,
Le sujet Mauvéine a 144 000 occurrences mais il est difficile de trouver le mode opératoire: je ne l'ai pas trouvé..
Re: Synthèse de la mauvéine
Publié : 26/05/2020, 15:33
par darrigan
Bonjour,
Sous le nom de mauvéine, on trouve en fait de nombreux dérivés du cation 7‐amino‐5‐phényl‐3‐(phénylamino)phénazin‐5‐ium.
Sur
ce site, on trouve ceci :
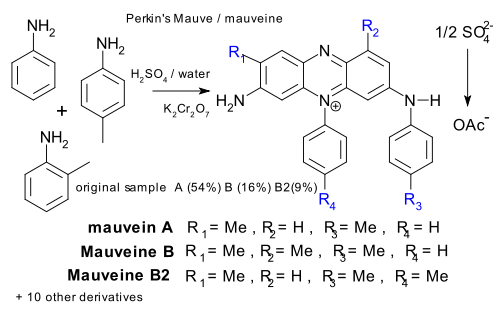
Voir aussi la
page de Wikipedia anglaise.
Pour faire des synthèses, il faut en général un montage à reflux, une système de filtration sur Büchner, une ampoule à décanter, etc., bref de la verrerie classique de laboratoire de chimie organique.
Mais c'est vrai que j'ai du mal à trouver la synthèse de cette mauvéine dans un article scientifique...

Ça doit bien exister quelque part !
Re: Synthèse de la mauvéine
Publié : 26/05/2020, 17:39
par ecolami
Bonjour,
Sur un autre forum quelq'u'un a trouve
https://www.researchgate.net/publicatio ... nd_details
Accès libre.
Synthesis of Mauveine. The general synthetic procedure used for mauveine consisted of mixing p-toluidine
(1.14 mmol, 122 mg), Mili-Q water (2.3 mL) and sulfuric acid (0.6 mL, 2.0 M) in a 25 mL glass vial13. The
reaction vial was magnetically stirred, and an ultrasound-enhanced dissolution was carried out. The reaction vial
was then heated gently using a controlled water bath until the reactants dissolved. After the complete dissolution
of p-toluidine, aniline (0.57 mmol, 0.052 mL), o-toluidine (0.55 mmol, 0.06 mL) and 30 mg of potassium dichromate
(K2Cr2O7) were added to 160 mL of water. Soon after the addition of K2Cr2O7, the solution turned purple.
This describes the synthesis for mauveine MV1, prepared using a 1:2:1 (mole) ratio of aniline, p-toluidine and
o-toluidine, respectively. The other samples followed the same synthetic method, with different proportions of
the starting materials and are labelled as MV2-6: 1:4:1, 1:4:2, 0:1:0, 1:10:5 and 1:10:10, respectively. The reaction
mixture was stirred and heated at controlled temperature (water bath) for two hours. At the end of the reaction
time, the liquid portion was discarded. The resulting dark solid was filtered using gentle suction filtration, and
washed with distilled water (slightly heated) until the washing solution becomes colorless. The remaining solid
was dried in an oven at ~110 °C for 30 min. It was then washed with petroleum ether until the washings became
colorless and dried again for 10 min at 110 °C. Finally, the remaining solid was washed with a 25% methanol/
water solution until the solution turned colorless. This aqueous/alcoholic solution was further evaporated. After
complete evaporation, 0.3 mL of methanol (100%) was added to the remaining solid and the sample transferred
with a filter pipet to a 5 mL vial. The liquid was carefully evaporated until its volume reduced to ca. 0.03 mL. This
final methanol solution contains the ultimate product, mauveine (in ca. 2 mg yield).

